2月7日,复宏汉霖(02696.HK)延续近期涨势,截至收盘,该股涨幅为8.38%,报20.05港元/股,成功录得5连涨,区间累计涨幅约19.63%。
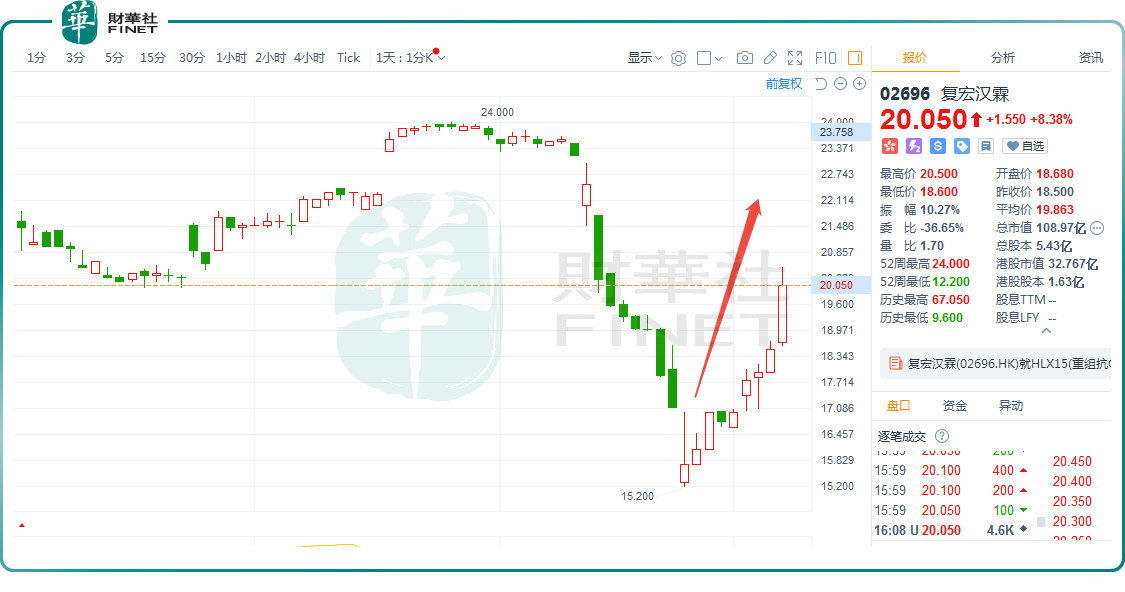
从消息面来看,复宏汉霖此轮涨幅,主要得益于公司产品最新进展消息的叠加催化效应。
2月2日,复宏汉霖发布公告称,近日,公司自主研发的Perjeta (帕妥珠单抗)生物类似药候选药HLX11(重组抗HER2结构域Ⅱ人源化单克隆抗体注射液)(HLX11)的生物制品许可申请(BLA)获美国食品药品管理局(FDA)受理。
据悉,HLX11是公司自主研发的帕妥珠单抗生物类似药,拟用于HER2阳性早期乳腺癌的新辅助/辅助治疗、HER2阳性转移性乳腺癌的治疗及与原研药药品标签相符的其他适应症。
紧接着,2月5日,复宏汉霖又传来喜讯。欧盟委员会已批准其自主研发的抗PD-1单抗斯鲁利单抗注射液(中国境内商品名:汉斯状)联合卡铂和依托泊苷适用于广泛期小细胞肺癌成人患者的一线治疗。
汉斯状在欧盟获批上市,将成为公司继曲妥珠单抗(中国境内商品名:汉曲优)之后,第二个在欧盟获批上市的产品,也成为欧盟首个批准用于广泛期小细胞肺癌治疗的抗PD-1单抗药品。复宏汉霖称,这意味着国际主流市场对汉斯状的认可,也将进一步提升公司产品的国际影响力。
2月6日,复宏汉霖再度发布公告称,与Dr. Reddy’s Laboratories SA("Dr.Reddy’s")订立一份许可协议,据此,公司向Dr.Reddy’s授出一项许可,供其于美国及约定的欧洲地区内及领域内开发、生产和商业化HLX15(重组抗CD38全人单克隆抗体注射液)的静脉注射制剂与皮下注射制剂。
HLX15是公司自主研发的达雷妥尤单抗生物类似药,计划用于治疗多发性骨髓瘤。该产品已于2024年6月在中国境内(不包括港澳台地区)成功完成1期临床研究。
复宏汉霖表示,本次与Dr. Reddy’s订立许可协议有助于深化公司产品的出海进程,进一步提升公司产品在国际市场的可及性和影响力。
作为国内生物类似药领域的领军企业,复宏汉霖自2019年成功开发上市国内第一款生物类似药“汉利康”以来,其产品商业化进展一直十分顺利。
截至目前,复宏汉霖已有6款产品在中国获批上市,4款产品在国际市场上获批上市。此外,公司还拥有多个处于临床Ⅲ期的项目,商业化前景明朗。
业界人士指出,凭借其多元的产品组合和现有的商业化优势,复宏汉霖正在不断推进已商业化产品的适应症拓展及市场拓展。汉曲优、汉斯状、汉贝泰等已实现商业化的产品,其商业价值尚未完全释放,未来的增长前景仍然可观。
1998-2025深圳市财华智库信息技术有限公司 版权所有
经营许可证编号:粤B2-20190408
粤ICP备12006556号